
Plusieurs médicaments-candidats à effet antiviral contre le Covid-19 ont donné de bons résultats dans le cadre des essais cliniques. Au nombre de ces médicaments, le Paxlovid qui a réussi à réduire de 89% le risque d’hospitalisation ou de décès lié au coronavirus. C’est le premier médicament oral contre le Covid-19 à être approuvé aux États-Unis et en Europe.
Le Paxlovid est un nouveau médicament antiviral oral recommandé chez les patients atteints d’une forme légère à modérée de Covid-19. Il est formé du nirmatrelvir, un nouvel inhibiteur de protéase (une enzyme jouant un rôle clé dans la réplication virale), et du ritonavir, une molécule utilisée pour diminuer le métabolisme du nirmatrelvir afin de prolonger son effet. Il est généralement administré à une dose de 300 mg (deux comprimés de 150 mg) de nirmatrelvir avec un comprimé de 100 mg de ritonavir, deux fois par jour pendant cinq jours. Une boîte contient cinq plaquettes alvéolées de Paxlovid, sous forme de comprimés de nirmatrelvir co-emballés avec des comprimés de ritonavir, fournissant toutes les doses requises pour un traitement complet de cinq jours.
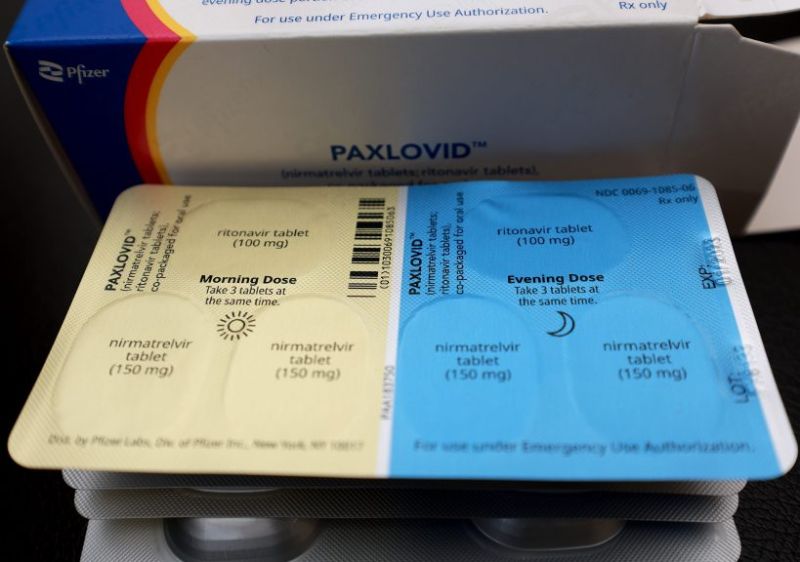 Le Paxlovid est un nouveau médicament antiviral oral recommandé chez les patients atteints d’une forme légère à modérée de Covid-19.
Le Paxlovid est un nouveau médicament antiviral oral recommandé chez les patients atteints d’une forme légère à modérée de Covid-19.
©Joe Raedle/Getty Images/AFP
L’octroi de son autorisation d’utilisation en urgence a été basé sur l’analyse intermédiaire des résultats de l’essai «Evaluation of Protease Inhibition for Covid-19 in High-Risk Patients» ou EPIC-HR (Évaluation de l’inhibition de protéase pour le Covid-19 chez des patients à haut risque). Il s’agit d’une étude de phase II/III randomisée, en double aveugle et contrôlée par placebo chez des patients adultes symptomatiques non hospitalisés, avec au moins un facteur de risque de progression vers une forme grave de la maladie. Les participants ayant préalablement contracté le Covid-19 ou ayant été vaccinés contre la maladie, ont été exclus.
Cette analyse intermédiaire est basée sur les données cliniques de 1 219 patients recevant aléatoirement soit le Paxlovid (607 patients) soit un placebo (612 patients). Durant un suivi de 28 jours, 7% des patients qui ont reçu le placebo ont été hospitalisés ou sont décédés (7 décès ultérieurs) alors que seulement 0,8% des patients ayant reçu le Paxlovid a été hospitalisé. Une réduction significative des hospitalisations ou des décès liés au Covid-19 a également été observée chez les patients traités dans les cinq jours suivant l’apparition des symptômes: 1% des patients ayant reçu le Paxlovid a été hospitalisé durant les 28 jours suivant la randomisation (6 patients hospitalisés sur 607, aucun décès), comparé à 6,7% des patients ayant reçu un placebo (41 patients hospitalisés sur 612, 10 décès ultérieurs).
L’analyse intermédiaire a finalement montré une réduction de 89% du risque d’hospitalisation ou de décès lié au Covid-19, quelle qu’en soit la cause, par rapport au placebo chez les patients traités dans les trois jours suivant l’apparition des symptômes (critère d’évaluation principal). Publiés en février 2022 dans le New England Journal of Medecine (NEJM), les résultats finaux de l’étude EPIC-HR, effectuée sur 2 246 patients, ont confirmé celles de l’analyse intermédiaire indiquant que le Paxlovid réduit le risque d’hospitalisation ou de décès de 89% (dans les trois jours suivant l’apparition des symptômes) et 88% (dans les cinq jours suivant l’apparition des symptômes) par rapport au placebo.
Il convient toutefois de noter que l’essai EPIC-HR a été mené avant l’émergence de la variante Omicron. Ainsi, la généralisation de ces résultats, à l’aune de cette nouvelle vague, pourrait être biaisée. En fait, le National Institutes of Health (NIH), aux États-Unis, recommande le Paxlovid comme traitement antiviral de premier choix chez les adultes non hospitalisés qui présentent un risque élevé de progression de la maladie, quel que soit leur statut vaccinal. Néanmoins, il a déclaré que les données sur l’efficacité de ce traitement contre la variante Omicron font défaut, malgré certains résultats encourageants issus de diverses études in vitro (sur des cellules, NDLR), soulignant une puissante inhibition de cette variante par le nirmatrelvir.
Une étude de cohorte rétrospective, publiée par Wong et al. le 24 août 2022 dans le Lancet, a permis quelque peu de trancher dans le vif. Se basant sur les données cliniques de patients hospitalisés atteints de Covid-19 et n’ayant pas eu besoin d’une oxygénothérapie, ce travail de recherche a démontré que l’initiation précoce des antiviraux oraux (molnupiravir ou nirmatrelvir/ritonavir) était associée à une réduction significative du risque de mortalité et de progression de la maladie. De plus, toujours selon cette même étude, les patients traités par l’un des deux antiviraux précités ont atteint une faible charge virale plus rapidement que les patients témoins, ce qui consolide l’hypothèse que le Paxlovid pourrait être actif contre la variante Omicron du SARS-CoV-2.
D’après une autre étude, également publiée le 24 août 2022 dans NEJM, des chercheurs fournissent des résultats tangibles sur l’efficacité du Paxlovid contre la variante Omicron. Les auteurs de cette publication ont étudié les données cliniques de 109 254 patients, dont la grande majorité avait été vaccinée contre le Covid-19, infectée par le SARS-CoV-2, ou les deux, et ont suivi l’évolution des taux d’hospitalisation et de mortalité, par tranche d'âge, dans cet échantillon. Parmi les 109 254 individus participant à l’étude, qui a été menée entre janvier et mars 2022, 3 902 avaient reçu le Paxlovid, et parmi les 42 819 patients âgés d’au moins 65 ans, 2 484 avaient reçu ce traitement. Le risque d’hospitalisation de ces derniers, vaccinés et non vaccinés, était réduit de 67% et leur risque de décès de 81%. Chez les 66 394 patients âgés de 40 à 64 ans (dont 1 418 patients traités), la réduction du risque d’hospitalisation ou de décès n’a pas été statistiquement significative. Par conséquent, les auteurs concluent qu’«aucune preuve de bénéfice» ne semble soutenir l’usage du Paxlovid chez les jeunes adultes âgés de moins de 65 ans.
Les résultats étaient également décevants quant à l’efficacité du Paxlovid dans le traitement des patients atteints de Covid-19, mais sans risque particulier de formes sévères. Cette problématique a été adressée dans le cadre d’un essai randomisé et contrôlé, intitulé «Evaluation of Protease Inhibition for COVID-19 in Standard-Risk Patients» ou EPIC-SR (Évaluation de l’inhibition de protéase pour le Covid-19 chez des patients à risque standard). L’analyse portant sur 1 153 patients, vaccinés ou non, a mis en évidence une réduction, statiquement non significative, de 51% du risque d’hospitalisation dans le groupe du Paxlovid. La réduction du nombre de consultations médicales liées au Covid-19 n’était pas non plus significative.
Ces résultats négatifs ont fait l’objet d’un communiqué de presse du laboratoire Pfizer, le 14 juin 2022, qui a décidé de suspendre son essai EPIC-SR, estimant que le risque d’hospitalisation dans cette population est trop faible pour poursuivre cette étude. La société américaine a, par contre, annoncé qu’elle «concentrera ses efforts sur la génération de données supplémentaires sur le Paxlovid dans les populations vulnérables», afin d’évaluer la possibilité d’administration de ce traitement oral chez des patients hospitalisés atteints d’une maladie grave, ou chez des patients immunodéprimés pour des durées plus longues.
À la lumière de toutes les études précitées, et bien d’autres, il est évident que le Paxlovid est loin d’être la panacée. Il permet certes de diminuer le nombre d’hospitalisations et de réduire considérablement le nombre de décès liés au Covid-19 chez certaines catégories de patients (notamment ceux souffrant de plusieurs maladies chroniques ou d’une maladie rare, et les individus âgés de plus de 65 ans avec des facteurs de comorbidité, comme l’obésité, le diabète et l’hypertension artérielle à titre d’exemple), mais il est loin d’être destiné à tous.
Par ailleurs, la Société française de pharmacologie et thérapeutique (SFPT) met en garde contre le potentiel important d’interactions médicamenteuses (dont certaines pourraient être fatales) que présente le Paxlovid, principalement dus à la présence du ritonavir. Le nouveau médicament serait, selon le rapport de février 2022 de la SFPT, contre-indiqué ou non recommandé dans 34 combinaisons médicamenteuses. De plus, la Haute autorité de santé (HAS) précise que l’antiviral est contre-indiqué chez les personnes ayant une insuffisance hépatique ou rénale sévère; une adaptation de la posologie serait, par contre, nécessaire chez les patients présentant une insuffisance rénale modérée. Toujours selon la HAS, le Paxlovid n’est pas recommandé chez les femmes enceintes et allaitantes, et «n’est pas destiné à être utilisé comme substitut à la vaccination contre le SRAS-CoV-2». Cela dit, attention de tomber dans les mêmes pièges du passé: le traitement miracle n’existe toujours pas.
Le Paxlovid est un nouveau médicament antiviral oral recommandé chez les patients atteints d’une forme légère à modérée de Covid-19. Il est formé du nirmatrelvir, un nouvel inhibiteur de protéase (une enzyme jouant un rôle clé dans la réplication virale), et du ritonavir, une molécule utilisée pour diminuer le métabolisme du nirmatrelvir afin de prolonger son effet. Il est généralement administré à une dose de 300 mg (deux comprimés de 150 mg) de nirmatrelvir avec un comprimé de 100 mg de ritonavir, deux fois par jour pendant cinq jours. Une boîte contient cinq plaquettes alvéolées de Paxlovid, sous forme de comprimés de nirmatrelvir co-emballés avec des comprimés de ritonavir, fournissant toutes les doses requises pour un traitement complet de cinq jours.
 Le Paxlovid est un nouveau médicament antiviral oral recommandé chez les patients atteints d’une forme légère à modérée de Covid-19.
Le Paxlovid est un nouveau médicament antiviral oral recommandé chez les patients atteints d’une forme légère à modérée de Covid-19.©Joe Raedle/Getty Images/AFP
L’octroi de son autorisation d’utilisation en urgence a été basé sur l’analyse intermédiaire des résultats de l’essai «Evaluation of Protease Inhibition for Covid-19 in High-Risk Patients» ou EPIC-HR (Évaluation de l’inhibition de protéase pour le Covid-19 chez des patients à haut risque). Il s’agit d’une étude de phase II/III randomisée, en double aveugle et contrôlée par placebo chez des patients adultes symptomatiques non hospitalisés, avec au moins un facteur de risque de progression vers une forme grave de la maladie. Les participants ayant préalablement contracté le Covid-19 ou ayant été vaccinés contre la maladie, ont été exclus.
Analyse intermédiaire
Cette analyse intermédiaire est basée sur les données cliniques de 1 219 patients recevant aléatoirement soit le Paxlovid (607 patients) soit un placebo (612 patients). Durant un suivi de 28 jours, 7% des patients qui ont reçu le placebo ont été hospitalisés ou sont décédés (7 décès ultérieurs) alors que seulement 0,8% des patients ayant reçu le Paxlovid a été hospitalisé. Une réduction significative des hospitalisations ou des décès liés au Covid-19 a également été observée chez les patients traités dans les cinq jours suivant l’apparition des symptômes: 1% des patients ayant reçu le Paxlovid a été hospitalisé durant les 28 jours suivant la randomisation (6 patients hospitalisés sur 607, aucun décès), comparé à 6,7% des patients ayant reçu un placebo (41 patients hospitalisés sur 612, 10 décès ultérieurs).
L’analyse intermédiaire a finalement montré une réduction de 89% du risque d’hospitalisation ou de décès lié au Covid-19, quelle qu’en soit la cause, par rapport au placebo chez les patients traités dans les trois jours suivant l’apparition des symptômes (critère d’évaluation principal). Publiés en février 2022 dans le New England Journal of Medecine (NEJM), les résultats finaux de l’étude EPIC-HR, effectuée sur 2 246 patients, ont confirmé celles de l’analyse intermédiaire indiquant que le Paxlovid réduit le risque d’hospitalisation ou de décès de 89% (dans les trois jours suivant l’apparition des symptômes) et 88% (dans les cinq jours suivant l’apparition des symptômes) par rapport au placebo.
Ère d’Omicron
Il convient toutefois de noter que l’essai EPIC-HR a été mené avant l’émergence de la variante Omicron. Ainsi, la généralisation de ces résultats, à l’aune de cette nouvelle vague, pourrait être biaisée. En fait, le National Institutes of Health (NIH), aux États-Unis, recommande le Paxlovid comme traitement antiviral de premier choix chez les adultes non hospitalisés qui présentent un risque élevé de progression de la maladie, quel que soit leur statut vaccinal. Néanmoins, il a déclaré que les données sur l’efficacité de ce traitement contre la variante Omicron font défaut, malgré certains résultats encourageants issus de diverses études in vitro (sur des cellules, NDLR), soulignant une puissante inhibition de cette variante par le nirmatrelvir.
Une étude de cohorte rétrospective, publiée par Wong et al. le 24 août 2022 dans le Lancet, a permis quelque peu de trancher dans le vif. Se basant sur les données cliniques de patients hospitalisés atteints de Covid-19 et n’ayant pas eu besoin d’une oxygénothérapie, ce travail de recherche a démontré que l’initiation précoce des antiviraux oraux (molnupiravir ou nirmatrelvir/ritonavir) était associée à une réduction significative du risque de mortalité et de progression de la maladie. De plus, toujours selon cette même étude, les patients traités par l’un des deux antiviraux précités ont atteint une faible charge virale plus rapidement que les patients témoins, ce qui consolide l’hypothèse que le Paxlovid pourrait être actif contre la variante Omicron du SARS-CoV-2.
Traitement efficace, mais…
D’après une autre étude, également publiée le 24 août 2022 dans NEJM, des chercheurs fournissent des résultats tangibles sur l’efficacité du Paxlovid contre la variante Omicron. Les auteurs de cette publication ont étudié les données cliniques de 109 254 patients, dont la grande majorité avait été vaccinée contre le Covid-19, infectée par le SARS-CoV-2, ou les deux, et ont suivi l’évolution des taux d’hospitalisation et de mortalité, par tranche d'âge, dans cet échantillon. Parmi les 109 254 individus participant à l’étude, qui a été menée entre janvier et mars 2022, 3 902 avaient reçu le Paxlovid, et parmi les 42 819 patients âgés d’au moins 65 ans, 2 484 avaient reçu ce traitement. Le risque d’hospitalisation de ces derniers, vaccinés et non vaccinés, était réduit de 67% et leur risque de décès de 81%. Chez les 66 394 patients âgés de 40 à 64 ans (dont 1 418 patients traités), la réduction du risque d’hospitalisation ou de décès n’a pas été statistiquement significative. Par conséquent, les auteurs concluent qu’«aucune preuve de bénéfice» ne semble soutenir l’usage du Paxlovid chez les jeunes adultes âgés de moins de 65 ans.
Les résultats étaient également décevants quant à l’efficacité du Paxlovid dans le traitement des patients atteints de Covid-19, mais sans risque particulier de formes sévères. Cette problématique a été adressée dans le cadre d’un essai randomisé et contrôlé, intitulé «Evaluation of Protease Inhibition for COVID-19 in Standard-Risk Patients» ou EPIC-SR (Évaluation de l’inhibition de protéase pour le Covid-19 chez des patients à risque standard). L’analyse portant sur 1 153 patients, vaccinés ou non, a mis en évidence une réduction, statiquement non significative, de 51% du risque d’hospitalisation dans le groupe du Paxlovid. La réduction du nombre de consultations médicales liées au Covid-19 n’était pas non plus significative.
Ces résultats négatifs ont fait l’objet d’un communiqué de presse du laboratoire Pfizer, le 14 juin 2022, qui a décidé de suspendre son essai EPIC-SR, estimant que le risque d’hospitalisation dans cette population est trop faible pour poursuivre cette étude. La société américaine a, par contre, annoncé qu’elle «concentrera ses efforts sur la génération de données supplémentaires sur le Paxlovid dans les populations vulnérables», afin d’évaluer la possibilité d’administration de ce traitement oral chez des patients hospitalisés atteints d’une maladie grave, ou chez des patients immunodéprimés pour des durées plus longues.
Haro sur l’automédication!
À la lumière de toutes les études précitées, et bien d’autres, il est évident que le Paxlovid est loin d’être la panacée. Il permet certes de diminuer le nombre d’hospitalisations et de réduire considérablement le nombre de décès liés au Covid-19 chez certaines catégories de patients (notamment ceux souffrant de plusieurs maladies chroniques ou d’une maladie rare, et les individus âgés de plus de 65 ans avec des facteurs de comorbidité, comme l’obésité, le diabète et l’hypertension artérielle à titre d’exemple), mais il est loin d’être destiné à tous.
Par ailleurs, la Société française de pharmacologie et thérapeutique (SFPT) met en garde contre le potentiel important d’interactions médicamenteuses (dont certaines pourraient être fatales) que présente le Paxlovid, principalement dus à la présence du ritonavir. Le nouveau médicament serait, selon le rapport de février 2022 de la SFPT, contre-indiqué ou non recommandé dans 34 combinaisons médicamenteuses. De plus, la Haute autorité de santé (HAS) précise que l’antiviral est contre-indiqué chez les personnes ayant une insuffisance hépatique ou rénale sévère; une adaptation de la posologie serait, par contre, nécessaire chez les patients présentant une insuffisance rénale modérée. Toujours selon la HAS, le Paxlovid n’est pas recommandé chez les femmes enceintes et allaitantes, et «n’est pas destiné à être utilisé comme substitut à la vaccination contre le SRAS-CoV-2». Cela dit, attention de tomber dans les mêmes pièges du passé: le traitement miracle n’existe toujours pas.
Lire aussi




Commentaires